Reportes de Casos
Síndrome de reacción a medicamento con eosinofilia y síntomas sistémicos (DRESS) asociado a levetiracetam: Reporte de caso
Drug reaction with eosinophilia and systemic symptoms (DRESS) associated with levetiracetam: Case report
Síndrome de reacción a medicamento con eosinofilia y síntomas sistémicos (DRESS) asociado a levetiracetam: Reporte de caso
Acta Médica Peruana, vol. 39, núm. 3, pp. 276-282, 2022
Colegio Médico del Perú

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional.
Recepción: 04 Agosto 2021
Aprobación: 01 Septiembre 2022
Resumen: El síndrome de hipersensibilidad a medicamentos, con eosinofilia y síntomas sistémicos (DRESS de sus siglas en inglés) es un síndrome muy infrecuente que se caracteriza por erupción dérmica, eosinofilia y compromiso sistémico. Inicialmente fue descrito asociado a medicamentos anticrisis (antiepilépticos), pero posteriormente ha sido descrito en asociación a otros medicamentos. Entre los medicamentos anticrisis, se ha descrito predominantemente su asociación a fármacos aromáticos o con estructura similar: fenitoína, carbamazepina, fenobarbital, oxcarbazepina y lamotrigina. Entre los medicamentos anticrisis no aromáticos, se ha descrito su presentación en algunos pacientes expuestos a gabapentina, zonisamida, valproato, rufinamida y raramente a levetiracetam. La severidad del síndrome se relaciona al tiempo de exposición al fármaco, por lo que su detección precoz es de vital importancia. Describimos el primer caso en nuestro país, de un paciente con DRESS inducido por levetiracetam y revisamos los infrecuentes reportes de DRESS en pacientes expuestos a levetiracetam descritos en la literatura.
Palabras clave: Síndrome de Hipersensibilidad a Medicamentos, Levetiracetam, Epilepsia, Perú.
Abstract: Drug reaction with eosinophilia and systemic symptoms (DRESS) is a very rare syndrome characterized by skin rash, eosinophilia and systemic compromise. This was initially described in association with antiseizures drugs, but later it was described in association with other drugs. Among antiseizure drugs, it has been described association with aromatic drugs as phenytoin, carbamazepine, phenobarbital, oxcarbazepine and lamotrigine; and non-aromatic antiseizure drugs as gabapentin, zonisamide, valproate, rufinamide and rarely to levetiracetam. The severity of the syndrome is related to the time of exposure to the drug, so early detection is of vital importance. We describe the first case in our country, of a patient with DRESS induced by levetiracetam, and we review the infrequent scientific reports of DRESS in patients exposed to levetiracetam.
Keywords: Drug Hypersensitivity Syndromes, DRESS Syndrome, Levetiracetam, Epilepsy, Peru.
INTRODUCCIÓN
El síndrome de hipersensibilidad a medicamentos, con eosinofilia y síntomas sistémicos (DRESS de sus siglas en inglés) es un síndrome muy infrecuente (incidencia estimada de 1/10.000 pacientes expuestos) que se caracteriza por: erupción dérmica, eosinofilia y compromiso sistémico (usualmente linfadenomegalias, compromiso hepático, pulmonar, renal y/o de miocardio). Inicialmente fue descrito asociado a medicamentos anticrisis (antiepilépticos), pero posteriormente ha sido descrito en asociación a neurolépticos atípicos, AINES, alopurinol, antituberculosos, antivirales y algunos antibióticos [1-4]. Entre los medicamentos anticrisis (MACs), se ha descrito predominantemente su asociación a fármacos aromáticos (fenitoína, carbamazepina, fenobarbital y oxcarbazepina) o que comparten en su estructura química una similitud (lamotrigina) [2-4]. Entre MACs no aromáticos, se ha descrito su presentación en algunos pacientes expuestos a gabapentina, zonisamida, valproato, rufinamida y raramente a levetiracetam [3-4]. Se ha reportado una mortalidad aproximada del 10 %, en especial asociada a falla hepática. La severidad del síndrome se relaciona al tiempo de exposición al MAC, por lo que su detección precoz es de vital importancia [4]. Describimos el primer caso en nuestro país, de un paciente con DRESS inducido por levetiracetam y revisamos los infrecuentes reportes de DRESS en pacientes expuestos a levetiracetam descritos en la literatura.
REPORTE DE CASO
Varón de 21 años, diestro, con antecedente de epilepsia focal estructural desde los 14 años y astrocitoma anaplásico orbitofrontal izquierdo diagnosticado y operado a los 15 años, luego recibió radioterapia y no presentó déficit focal neurológico secuelar. Posterior a ello se incrementó la frecuencia de las crisis focales. Entonces; estas se presentaban con compromiso de conciencia que iniciaban con aura de “malestar inespecífico” y progresaban a detención del comportamiento, con pérdida del contacto, automatismos orales y manuales izquierdo. Desde los 13 a los 15 años recibió acido valproico 2g/día sin alcanzar un adecuado control de las crisis (4 crisis semanales), por lo que le rotaron a fenitoína 300mg/día. Ingresó para estudio prequirúrgico de cirugía de epilepsia: realización de video- electroencefalograma (VEEG) prolongado, resonancia magnética (RM) de encéfalo y tomografía por emisión de positrones (PET) cerebral (Figura 1). A su ingreso se encontraba recibiendo levetiracetam y fenitoína en la dosis referida. El levetiracetam a dosis de 3g/día, lo había iniciado dos semanas antes del ingreso con mejoría parcial de la frecuencia de crisis: eventos casi diarios a 2-3 veces por semana.
Con la finalidad de capturar crisis durante la telemetría, se retiró la fenitoína. Se realizó el VEEG de 78 horas manteniendo levetiracetam, capturándose 3 crisis y determinando la zona epileptógena en región temporal anterior izquierda (Figura 1G), la RM de encéfalo evidenció lesión tumoral quística temporal anterior izquierda que realzaba con el gadolinio, además de una encefalomalacia orbitofrontal izquierda (Figura 1A-D). La PET cerebral inter-ictal evidenció hipometabolismo temporal izquierda (Figura 1E y F). Durante el último día de telemetría, encontrándose aún solo con levetiracetam, presentó un pico febril (38 °C), asociado a eritema morbiliforme confluente en tronco, rostro, cuello y extremidades, asociado a prurito intenso (Figura 2 A-F). Las otras funciones vitales fueron normales. Al examen físico, solo encontramos linfadenomegalias cervicales y submandibulares. A la administración de clorfeniramina solo disminuyó parcialmente el prurito, se sospechó de una reacción a medicamento y se solicitó analítica evidenciando leucocitosis (16,780/uL) con linfocitos atípicos (2 %), eosinofilia (33.6 %; 5,640/uL), elevación de enzimas hepáticas (TGP 534 UI/L, TGO 252 UI/ L, fosfatasa alcalina 475 UI/L, las bilirrubinas fueron normales), leve elevación de creatinina (1.35mg/dL). Paralelamente se excluyó procesos infecciosos bacterianos, virales, parasitarios y colagenopatías. Entre otros exámenes, la serología para hepatitis, TORCH, virus Epstein Bar (VEB) y herpesvirus humano 6 (HHV-6) fue negativa. El ELISA VIH y VDRL fueron negativos. La ecografía de abdomen y radiografía de tórax fueron normales.
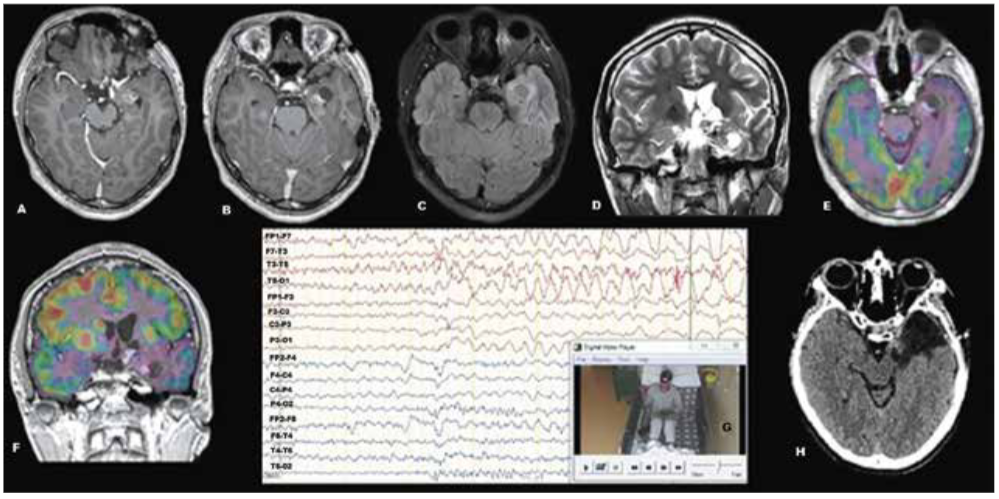
Figura 1.
Estudio prequirúrgico para cirugía de epilepsia. RM de encéfalo: tumor quístico temporal anteromesial izquierdo y malacia orbitofrontal izquierda (A,B,C,D). PET scan interictal: extenso hipometabolismo izquierdo a predominio mesial (E,F). VideoEEG ictal: zona epileptógena temporal anterior – media izquierda (G). Tomografía cerebral postoperatoria: lobectomía temporal izquierda.
| Autor | Edad (años) | Sexo | Cuadro clínico | Analítica | Regi-SCAR | Tiempo de exposición | Tiempo de remisión desde el retiro | Tratamiento |
| Lens S (España 2010) | 18 | Mujer | Fiebre, rash, edema facial, faringitis y hepatitis aguda severa con encefalopatía hepática y neumonitis | Eosinofilia 4700/uLAST/ ALT=1145/1357 UI/LBilirrubinas 5.4mg/dL | 6 | 21 días | 8 días | Metilprednisolona1.8mg/Kg/día |
| Gómez Zorrilla(España 2012) | 31 | Varón | Fiebre, rash, neumonitis | Leucocitosis 11,900/μLEosinófilos 0.9% ALT/ AST/LDH = 60/ 53/ 516 UI/L | 6 | 49 días | 12 días | Dexametasona 12 mg /día |
| Hall (USA 2013) | 18 | Varón | Fiebre, rash, neumonitis, hepatitis | Leucocitos 7,900/uLEosinófilos 4% AST =778 IU/L, ALT = 1274 IU/L | 5 | 35 días (asociado a fenitoína) | No reporta | Dexametasona sin especificar dosis |
| Eleni K(Grecia 2013) | 53 | Varón | Fiebre 38.2C, rash, proctitis | Leucocitosis 28,0000/uL,eosinofilia 14,860 mm³ (50%),AST= 101 UI/L, ALT = 172 UI/L. | 5 | 16 días | 10 días | Metilprednisolona 1mg/kg |
| Jones R(USA 2014) | 64 | Varón | Fiebre 38.7C, rash | Leucocitos 8,400/uLeosinofilia 3,000/uLALT = 64 UI/L. | 6 | 6.5 días | 4 días | Metilprednisolona 125mg EV cada 8 horas |
| Bayram A(Turquía 2015) | 9 | Mujer | Fiebre, rash, edema facial, faringitis exudativa, linfadenopatías cervicales, hepatomegalia dolorosa, neumonitis | Leucocitosis 17.200/uL, Eosinofilia 2.900/uL, Trombocitopenia 104.000/uLAST 314 UI/L, ALT 224 UI/L bilirrubina 2.9 mg/dL | 7 | 19 días | 13 días | Prednisolona 1mg/kg/día |
| Dar(India 2016) | 40 | Varón | Fiebre, rash, linfadenomegalia cervicales y axilares | Leucocitos: 8200/uL (Linfocitos 21%, Eosinófilos 4% ), ALT 714 UI/L, AST 164 UI/L | 4 | 7 días | 6 días | Dexametasona 4mg EV cada 8 horas |
| Moreno D(España 2016) | 56 | Varón | Fiebre, rash. | Eosinofilia 1400/ uL, ALT y Fosfatasa Alcalina 775 UI/L y 620 UI/L, bilirrubina total 4,2 mg/dL | 3 | 2 meses | >48 horas | Corticoide EV sin especificar dosis y tipo |
| Singh T(USA 2019) | 36 | Mujer | Fiebre, rash, linfadenopatías cervicales y submandibulares, colecistitis, faringitis, compromiso pulmonar | Eosinófilos 4%, ALT 1231, AST 1026 y Fosfatasa alcalina 362UI/L | 6 | 4 semanas(asociado a lamotrigina) | 8 semanas | Supresión FAE |
| Nogueiras(España 2019) | 50 | Varón | Fiebre, rash. | Eosinofilia (12%) | 2 | 2 dosis de levetiracetam EV (presentó luego reacción cruzada con fenitoina y valproato) | desconocido | Corticoide sin especificar dosis y tipo |
Se planteó el diagnóstico de DRESS y se suspendió el levetiracetam. Se inició clobazam a 30mg/día, se administró dexametasona 18mg/día EV por 5 días y se continuó con prednisona 1 mg/kg /día VO. A la semana hubo una mejoría significativa de la analítica y al décimo día mejoró la reacción dérmica, progresando a una dermatitis exfoliativa para luego resolverse completamente (Figura 2 G). Debido a que presentó tres crisis epilépticas focales en este periodo a pesar de recibir clobazam, se añadió topiramato a 300 mg/día. Se decidió no reiniciar fenitoína, debido a la posibilidad de reacción cruzada del DRESS con otros MACs. Los corticoides se mantuvieron por dos meses con una reducción gradual. Posteriormente el paciente fue intervenido de una lobectomía temporal anterior izquierda (Figura 1H) y quedó medicado con topiramato y clobazam; diagnosticándosele un ganglioglioma temporal anteromesial izquierdo por anatomopatología. Actualmente se encuentra en Engel Ib.
DISCUSIÓN
En 1996, Bocquet et al. acuñaron el acrónimo DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms) para redefinir el fenómeno previamente conocido como síndrome de hipersensibilidad a medicamentos, una reacción idiosincrática a fármacos [5]. Inicialmente fue asociado a medicamentos anticrisis (MACs), pero posteriormente se ha descrito en asociación a neurolépticos atípicos, AINES, hidroxicloroquina, alopurinol, antituberculosos, algunos antivirales y algunos antibióticos como β – lactámicos, vancomicina, sulfas y tetraciclinas [1-4]. Entre los MACs, se ha descrito predominantemente su asociación a fármacos aromáticos (fenitoína, carbamazepina, oxcarbazepina y fenobarbital) o que comparten similitud en su estructura química (lamotrigina). Es muy infrecuente su reporte en casos expuestos a MACs no aromáticos como el levetiracetam [3-4].
Clásicamente, en el cuadro clínico del DRESS se ha descrito fiebre (>90 % de los casos), rash cutáneo maculopapular o morbiliforme, confluente, eritematoso, centrífugo de tronco a extremidades (>70 % de los casos), eosinofilia, linfadenomegalias y compromiso sistémico. La afectación sistémica puede comprender: disfunción hepática (hasta 60 % de los casos) que puede expresarse desde elevación de enzimas hasta hepatitis fulminante, pulmonar (neumonitis) y/o renal (nefritis intersticial). Con menor frecuencia han sido descritos compromisos digestivos, cardiacos y de tiroides. Paraclínicamente, además de la elevación de la enzimas hepáticas y eosinofilia, se describen otras alteraciones hematológicas, siendo las más frecuentes la leucocitosis y presencia de linfocitos atípicos; aunque también se han reportado anemia y trombocitopenia [1-4]. En nuestro caso encontramos: fiebre, erupción cutánea, lingadenomegalias periféricas, eosinofilia, linfocitos atípicos, compromiso renal y hepático.
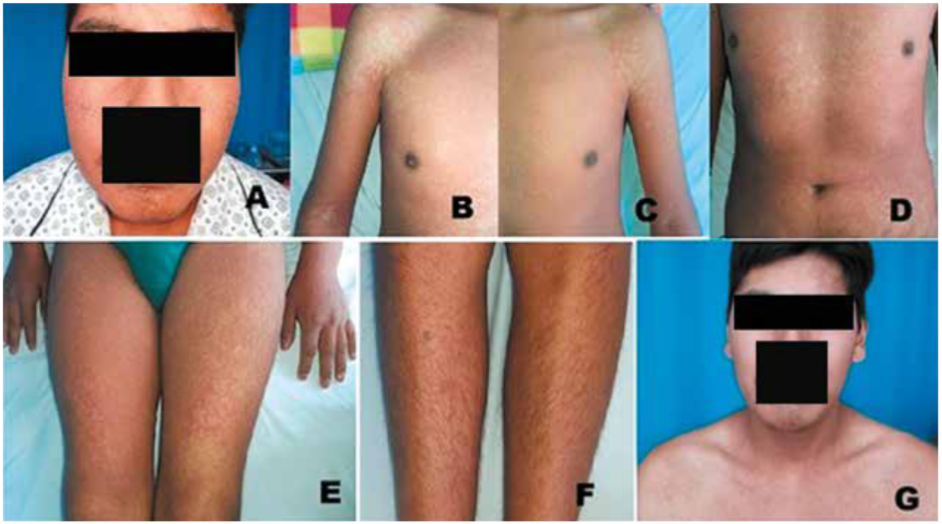
Figura 2.
Erupción cutánea morbiliforme como parte de DRESS. Fase inicial de DRESS (A – F). Fase de recuperación (G).
A propósito de nuestro caso, realizamos una búsqueda en PubMED/Medline, Scielo, Google Scholar y encontramos solo 10 casos reportados de DRESS inducido por levetiracetam (tabla 1). Respecto a la edad y sexo, la mayoría fueron adultos jóvenes varones, como el caso de nuestro paciente que tenía 21 años; la edad promedio fue d 37.5 años (rango de 9 a 64 años) y 7 de los 10 casos fueron varones. Respecto al cuadro clínico, de forma similar a nuestro caso, todos los pacientes reportados presentaron fiebre, erupción dérmica y 9 pacientes tuvieron compromiso hepático manifestado desde una leve elevación de transaminasas hasta una hepatitis aguda severa. Nuestro paciente, además, presentó compromiso renal leve, manifestado por una elevación de la creatinina que se resolvió tras la administración de corticoides. En ninguno de los casos descritos previamente se reportó compromiso renal; en tanto que en 5 pacientes hubo compromiso pulmonar, en un caso se reportó proctitis y en un caso se describió colecistitis. En 3 de los 10 casos descritos hubo linfadenomegalias periféricas y en 9 casos hubo eosinofilia, como en nuestro paciente [6-15].
Actualmente, de forma consensuada, se utiliza la puntuación del Registro Internacional de Reacciones Adversas Severas (RegiSCAR de sus siglas en inglés: international registry of severe cutaneous adverse reactions) (Tabla 2) para facilitar un diagnóstico precoz y suspender oportunamente el medicamento, pues se ha correlacionado la severidad del síndrome al tiempo de exposición. Una puntuación mayor a 5 clasifica al caso como definitivo, nuestro caso tuvo 8 puntos y por tanto clasificó como DRESS definitivo [16]. Cinco de los 10 casos reportados fueron clasificados como definitivos y solo 2, como posibles según el RegiSCAR [6-15]. Las manifestaciones clínicas del DRESS, generalmente aparecen entre dos y ocho semanas tras el inicio del tratamiento y se ha descrito presentación por reacción cruzada entre MACs aromáticos hasta en un 75 % [1-4]. De los 10 casos reportados tras exposición a levtiracetam, en la mayoría de los casos ocurrió entre 7 y 30 días tras su administración [6-15]. En nuestro caso el DRESS ocurrió tras 16 días de exposición.
Aunque la fisiopatogenia aún no está clara; se ha postulado que el DRESS sería generado por una reacción de hipersensibilidad inmune tipo IV. Esta reacción sería desencadenada por metabolitos intermedios (epóxidos de areno o arenóxidos) del fármaco anticrisis, luego de su metabolismo por la isoenzima citocromo P450 y que normalmente serian depurados por el epóxido hidrolasa. La deficiencia hereditaria/genética de la función de esta enzima podría predisponer a algunos pacientes a la presentación de DRESS. La predisposición genética estaría mediada por determinadas variantes o polimorfismos del HLA. La baja incidencia del síndrome sugiere esta predisposición genética. Adicionalmente, se ha reportado una fuerte asociación entre el DRESS y reactivaciones de ciertos herpesvirus (HHV-6, CMV y VEB), para lo cual se ha planteado una compleja interacción entre estos virus, la respuesta inmune frente a virus y respuestas inmunes especificas a determinados medicamentos. En nuestro caso no se encontró tal asociación [2-3].
| Parámetro | No | Si | Desconocido |
| Fiebre (> 38.5 °C) | -1 | 0 | -1 |
| Linfadenomegalias (≥2 lugares, >1 cm) | 0 | 1 | 0 |
| Linfocitos atípicos | 0 | 1 | 0 |
| Eosinófilos | |||
| 700-1499 /uL o 10-19.9% | 0 | 1 | 0 |
| ≥ 1500 /uL o ≥20% | 0 | 2 | 0 |
| Erupción dérmica | |||
| Extensa > 50% de superficie corporal | 0 | 1 | 0 |
| Rash cutáneo compatible con DRESS (por lo menos 2 de: edema, infiltración, púrpura, descamación) | -1 | 1 | 0 |
| Biopsia que sugiera DRESS | -1 | 0 | 0 |
| Compromiso de órganos internos | |||
| Uno | 0 | 1 | 0 |
| Dos o más | 0 | 2 | 0 |
| Resolución en más de 15 días | -1 | 0 | -1 |
| ≥ 3 investigaciones biológicas con resultados negativos que excluyan otros diagnósticos alternativos | 0 | 1 | 0 |
Levetiracetam tiene una estructura química diferente a los MACs aromáticos, su metabolismo es independiente de la isoenzima citocromo P450 y su mecanismo de acción es completamente diferente a los MACs habitualmente relacionados a DRESS. Levetiracetam actúa principalmente mediante su acción sobre proteínas 2A de vesículas sinápticas y secundariamente sobre los canales de calcio tipo N. Debido a estas diferencias respecto a los MACs aromáticos, el DRESS inducido por levetiracetam podría ser generado por un mecanismo diferente al descrito, que aún es desconocido [7]. Así mismo queda la interrogante de si pudiese ocurrir en forma cruzada DRESS a levetiracetam en pacientes que presentaron previamente DRESS a MACs aromáticos como la carbamazepina o fenitoína. Bajo esta duda, en nuestro caso podríamos haber tomado la decisión de reiniciar fenitoína a nuestro paciente, luego de haberle suspendido para la realización de la telemetría. Sin embargo, ante la incertidumbre y luego de conversar con el paciente sobre dicha situación, se decidió por no reiniciar fenitoína y utilizar MACs no relacionados a DRESS como clobazam y topiramato.
En base a experiencia de expertos, el tratamiento de elección consiste en la supresión del fármaco y la administración de corticoides endovenosos a dosis de 1-1.5 mg/kg de prednisona o su equivalente hasta la resolución completa del rash y luego una reducción gradual lenta. En casos leves sin compromiso sistémico, se ha sugerido que podría prescindirse del tratamiento con corticoides orales o parenterales. Aun cuando no hay un consenso sobre la duración, algunos expertos recomiendan realizar una reducción gradual muy lenta a lo largo de 2 a 6 meses para evitar recaídas; en nuestro caso seguimos tal conducta. Complementariamente, se puede usar antipiréticos, antihistamínicos y fluidos. Si no se observa respuesta a corticoides, se ha sugerido el uso de inmunoglobulina endovenosa, recambio plasmático, rituximab o inmunosupresores como ciclofosfamida, ciclosporina o micofenolato [3-4]. En la mayoría de los casos reportados de DRESS asociado a uso de levetiracetam, como en el nuestro, se usó de inicio dexametasona o metilprenisolona endovenosa y no se requirió de inmunoglobulina u otros inmunosupresores/ inmunomoduladores. En un caso de los 10 revisados, el cuadro clínico remitió solo con la supresión del levetiracetam. El tiempo de remisión tras el retiro fue variable y fluctuó entre 2 días y 8 semanas [6-15]. En nuestro paciente presentó remisión tras 10 días del retiro de levetiracetam.
En conclusión, debemos tener presente la ocurrencia de esta reacción idiosincrática, no solo cuando administramos MACs aromáticos a nuestros pacientes, sino también cuando usamos levetiracetam, debemos retirar oportunamente el fármaco y usar precozmente corticoides cuando hay compromiso sistémico para evitar cuadros de gran severidad.
REFERENCIAS BIBLIOGRÁFICAS
1. Cardones AR. Drug reaction with eosinophilia and systemic symptoms (DRESS) síndrome. Clin Dermatol. 2020; 38(6):702-711. https://doi.org/10.1016/j.clindermatol.2020.06.008.
2. Shiohara T, Mizukawa Y. Drug-induced hypersensitivity syndrome (DiHS)/drug reaction with eosinophilia and systemic symptoms (DRESS): An update in 2019. Allergol Int. 2019; 68(3):301-308. https://doi.org/10.1016/j.alit.2019.03.006.
3. Cho YT, Yang CW, Chu CY. Drug Reaction with Eosinophilia and Systemic Symptoms (DRESS): An Interplay among Drugs, Viruses, and Immune System. Int J Mol Sci. 2017; 18(6):1243. https://doi. org/10.3390/ijms18061243.
4. Martínez-Cabriales SA, Rodríguez-Bolaños F, Shear NH. Drug Reaction with Eosinophilia and Systemic Symptoms (DReSS): How Far Have We Come? Am J Clin Dermatol. 2019; 20(2):217-236. https://doi.org/10.1007/s40257-018-00416-4.
5. Bocquet, H.; Bagot, M.; Roujeau, J.C. Drug-induced pseudolymphoma and drug hypersensitivity síndrome (drug rash with eosinophilia and systemic symptoms: DRESS). Semin Cutan Med Surg. 1996; 15:250–257. https://doi.org/10.1016/s1085-5629(96)80038-1.
6. Lens S, Crespo G, Carrion J, Miquel R, Navasa M. Severe acute hepatitis in DRESS síndrome: Report of two cases. Annals of Hepatology. 2010; 9(2):198-201. https://doi.org/10.1016/S1665-2681(19)31663-1.
7. Gómez-Zorrilla S, Ferraz AV, Pedrós C, Lemus M, Peña C. Levetiracetam-induced drug reaction with eosinophilia and systemic symptoms syndrome. Ann Pharmacother. 2012; 46(7- 8):e20. https://doi.org/10.1345/aph.1r084.
8. Hall, D.J., Fromm, J.S. Drug reaction with eosinophilia and systemic symptoms syndrome in a patient taking phenytoin and levetiracetam: a case report. J Med Case Reports. 2013-, 7( 2): 1-5. https://doi.org/10.1186/1752-1947-7-2.
9. Eleni K. Dress syndrome induced by levetiracetam. J Eur Acad Dermatol Venereol. 2015;29(2):377-378. https://doi.org/10.1111/ jdv.12346.
10. Jones RT, Evans W, Mersfelder TL, Kavanaugh K. Rare Red Rashes: A Case Report of Levetiracetam-Induced Cutaneous Reaction and Review of the Literature. Am J Ther. 2016; 23(3):e944-6. DOI: 10.1097/MJT.0000000000000105.
11. Bayram AK, Canpolat M, Çınar SL, Tahan F, Gumus H, Kumandaş S, Per H. Drug Reaction with Eosinophilia and Systemic Symptoms Syndrome Induced by Levetiracetam in a Pediatric Patient. J Emerg Med. 2016;50(2):e61-6. DOI: 10.1016/j.jemermed.2015.10.004.
12. Dar WR, Sofi N, Latief M, Dar IA, Kasana BA. Levetiracetam Induced Drug Reaction with Eosinophilia and Systemic Symptom Syndrome. Indian J Dermatol. 2016;61(2):235. Disponible en: https://www.e- ijd.org/text.asp?2016/61/2/235/177777.
13. Moreno Diaz J, Martinez Huguet C, Arazo Garces P. Sindrome de DRESS asociado a Levetiracetam. Galicia Clin 2016; 77 (3): 134-136. Disponible en: https://galiciaclinica.info/PDF/37/874.pdf.
14. Singh T, Niazi M, Karri K, Rudikoff D, Gonzalez E. A Rare Case of DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms) Syndrome with Cholecystitis in a Patient on Levetiracetam. Cureus. 2019; 11(3):e4245. DOI: 10.7759/cureus.4245.
15. Nogueira R. Revisión del síndrome de hipersensibilidad a anticonvulsivantes, a propósito de un caso clínico complejo. Med Clin Pract. 2019; 2(3):51–53. Disponible en: http:// www.scielo.edu.uy/scielo.php?script=sci_arttext&pid=S1688- 12492016000100007&lng=es.
16. Kardaun SH, Sidoroff A, Valeyrie-Allanore L, et al. Variability in the clinical pattern of cutaneous side-effects of drugs with systemic symptoms: does a DRESS syndrome really exist? Br J Dermatol 2007;156: 609-11. https://doi.org/10.1111/j.1365- 2133.2006.07704.x
Notas de autor
elliotba@hotmail.com